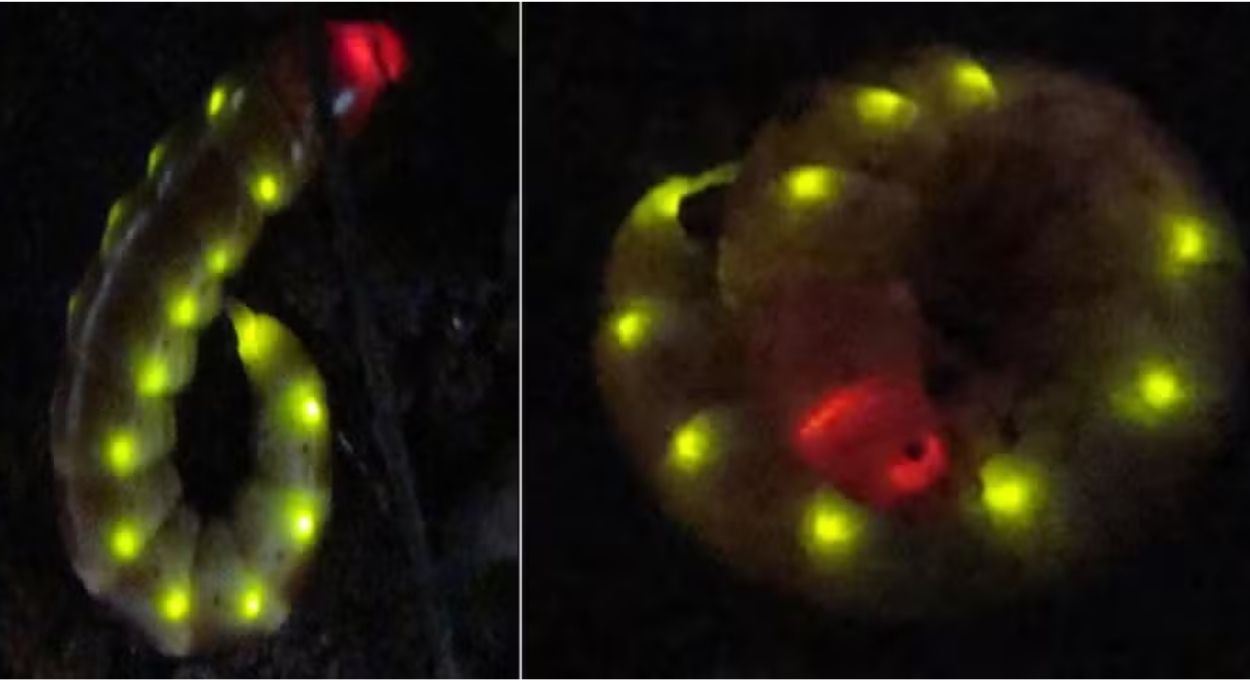
No chão da mata, entre folhas secas e raízes, uma larva de besouro se move sob a escuridão emitindo uma luz que nenhum outro organismo terrestre consegue replicar: o vermelho. Discreta, quase invisível para predadores e presas, a larva-trenzinho — nome popular da espécie Phrixotrix hirtus — carrega na cabeça uma característica que intrigou cientistas por décadas e agora está no centro de um dos avanços mais relevantes da biotecnologia brasileira. Pesquisadores da Universidade Federal de São Carlos (UFSCar) desenvolveram um sistema de bioluminescência baseado em uma versão mutante da enzima dessa larva, capaz de detectar tumores, infecções e processos metabólicos em tempo real nas camadas mais profundas do organismo de mamíferos.
A descoberta não surgiu do acaso. Ela é resultado de mais de 25 anos de pesquisa acumulada sobre a bioquímica da Phrixotrix hirtus, espécie que ocorre quase exclusivamente no Brasil e que representa, até hoje, o único caso documentado de bioluminescência vermelha em um organismo terrestre.
A enzima que a ciência brasileira colocou no mapa
A trajetória começa no fim da década de 1990, quando o bioquímico Vadim Viviani, pesquisador da UFSCar, clonou pela primeira vez a enzima responsável pela luz vermelha da larva-trenzinho durante um pós-doutorado no Japão. A molécula pertence à família das luciferases, enzimas que catalisam reações de oxidação de compostos chamados luciferinas, gerando bioluminescência como subproduto. O que diferencia a luciferase da Phrixotrix hirtus das demais é justamente o comprimento de onda da luz que ela produz, acima de 650 nanômetros, dentro da faixa do chamado vermelho distante.
Esse detalhe, aparentemente técnico, tem implicações práticas enormes. Os organismos de mamíferos são ricos em hemoglobina, mioglobina e melanina, pigmentos que absorvem a luz nas faixas azul, verde e verde-amarelo, que são exatamente as cores produzidas pela grande maioria das luciferases conhecidas e comercialmente disponíveis. Na prática, essa absorção impede que a bioluminescência atravesse os tecidos com eficiência, limitando o uso da técnica em modelos animais fundamentais para a pesquisa biomédica, como ratos, camundongos e coelhos.
“Por isso existe a necessidade de sistemas que emitem luz vermelha, especialmente na faixa do vermelho distante. A luz vermelha passa facilmente por esses tecidos, inclusive tecido ósseo”, explica Viviani.
Como a larva-trenzinho ilumina sem ser vista
Para entender por que essa larva evoluiu para emitir luz vermelha, é preciso observar seu comportamento no habitat natural. A Phrixotrix hirtus possui lanternas verdes espalhadas pelas laterais do corpo, que acendem quando o animal é tocado ou se sente ameaçado, funcionando como um mecanismo de defesa contra predadores. A luz vermelha da cabeça, contudo, tem uma lógica diferente. Pesquisadores suspeitam que ela funcione como uma lanterna de caça, iluminando o ambiente noturno enquanto a larva vasculha o folhiço em busca de alimento, sem ser detectada por presas nem por predadores, já que a maioria dos organismos terrestres possui baixíssima sensibilidade à luz nessa faixa do espectro.
Esse comportamento natural, refinado pela evolução ao longo de milhões de anos, foi exatamente o ponto de partida para a solução tecnológica desenvolvida na UFSCar. Se a luz vermelha atravessa tecidos sem ser absorvida pelos pigmentos naturais, o mesmo princípio poderia ser aplicado para enxergar processos biológicos escondidos nas camadas mais profundas de um organismo vivo.
Da biodiversidade ao laboratório: engenharia genética e química combinatória
O avanço mais recente do grupo foi publicado na revista Chemical & Biomedical Imaging e descreve um sistema de bioluminescência capaz de atingir comprimentos de onda de até 660 nm, mais brilhante, estável e duradouro do que o sistema desenvolvido pelo próprio grupo em 2021, que já era superior aos disponíveis no mercado.
O resultado deriva da combinação de duas estratégias: engenharia genética aplicada à luciferase da larva-trenzinho e química combinatória para modificar a luciferina sintética que serve de substrato à enzima. O primeiro autor do estudo é o biólogo Gabriel Felder Pelentir, doutorando orientado por Viviani no Programa de Pós-Graduação em Biotecnologia da UFSCar.
“A gente escolhe o aminoácido que quer mudar e faz todas as mutações de aminoácidos que podem ocorrer ali, para avaliar quais são as melhores”, detalha Pelentir.
O trabalho foi possível graças a uma descoberta anterior, realizada entre 2015 e 2019 pela então doutoranda Vanessa Rezende Bevilaqua, também orientada por Viviani. Em sua pesquisa, Bevilaqua demonstrou que a luciferase da Phrixotrix hirtus possui um sítio ativo maior do que o das luciferases clássicas de vagalumes, o que abre espaço para acomodar moléculas de luciferina sinteticamente modificadas. Esse conhecimento estrutural foi determinante para que a equipe pudesse redesenhar a enzima por engenharia genética e ampliar ainda mais sua capacidade de emitir luz no vermelho distante.
Resultado supera o padrão comercial mais usado no mundo
Os testes realizados em células de mamíferos confirmaram que o novo sistema supera o Akaluc/AkaLumine, considerado atualmente o padrão de referência para aplicações de imageamento biológico na faixa do vermelho distante e do infravermelho próximo. A superação de um benchmark comercial consolidado é um indicador relevante de maturidade tecnológica, especialmente em um campo tão competitivo quanto o da biotecnologia aplicada às ciências biomédicas.
As aplicações práticas são amplas. Como biossensores ou genes-repórteres, as luciferases sinalizam a expressão de genes específicos, detectam variações de pH, identificam bactérias patogênicas e rastreiam processos metastáticos em tempo real, sem a necessidade de procedimentos invasivos. Em pesquisas com modelos animais, essa capacidade de observar o que acontece nas camadas profundas do organismo representa um salto metodológico considerável, reduzindo tanto o tempo de diagnóstico experimental quanto o número de animais necessários em cada protocolo.
Além da biomedicina, as luciferases desenvolvidas pelo grupo da UFSCar também encontram aplicação como biossensores ambientais, na detecção de poluentes e substâncias tóxicas em diferentes ecossistemas.
Brasil abriga a maior diversidade de insetos bioluminescentes do planeta
O contexto que torna esse tipo de pesquisa possível no Brasil não é coincidência. O país abriga aproximadamente 500 das 2.500 espécies de insetos bioluminescentes descritas no mundo, ou seja, cerca de um quinto do total global. Viviani, que coordena o maior banco de luciferases do mundo na UFSCar, com cerca de 20 enzimas selvagens isoladas da biodiversidade brasileira e centenas de versões mutantes, ressalta que esse número ainda subestima a riqueza real do território nacional.
“O número deve ser bem maior, porque tem muitas espécies que ainda não foram descobertas ou não foram descritas nem na Mata Atlântica nem no Cerrado, e muito menos na Amazônia. E a gente sabe que não é só bonito; tem utilidade para a ciência e, claramente, para inovação tecnológica”, afirma o pesquisador.
Várias das moléculas desenvolvidas pelo laboratório já foram patenteadas, consolidando a UFSCar como referência global em pesquisa aplicada sobre bioluminescência. A pesquisa contou com apoio da FAPESP e com colaboração de cientistas da Universidade de Eletro-Comunicações de Tóquio, que contribuíram com a síntese das luciferinas utilizadas nos experimentos.
O próximo passo do grupo é avançar nos testes em modelos animais vivos, ampliando a validação do sistema para aplicações in vivo mais complexas e aproximando a tecnologia de possíveis usos clínicos e diagnósticos no futuro.